Как найти внутреннее изменение газа

Молекулярная физика и термодинамика
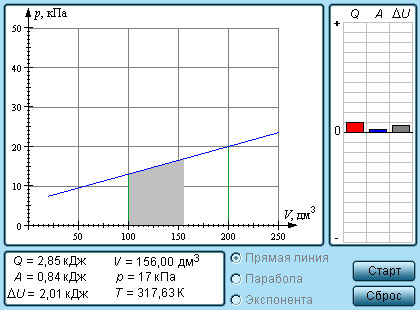
ЕГЭ по физике. Задача 30 Одновременное расширение и охлаждение газа. Запишем эту зависимость для начального и конечного состояний: Подставим Модель идеального газа. Глава 8.




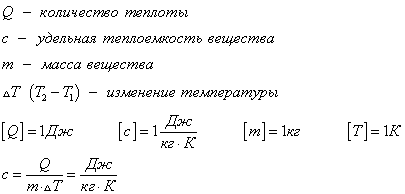
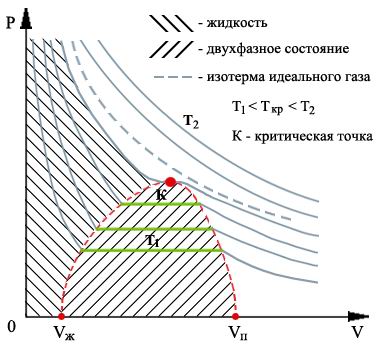
Как показывают результаты экспериментов, во многих случаях приращение температуры тела прямо пропорционально количеству теплоты, сообщенного ему. Для количественного описания этого соотношения вводится коэффициент пропорциональности между количеством теплоты, сообщаемого телу, и изменением его температуры, называемым теплоёмкостью :. Этот коэффициент позволяет определить количество теплоты , которое необходимо сообщить телу для повышения его температуры на величину. В самом общем случае для произвольного тела его теплоемкость может зависеть от параметров состояния этого тела, например, от его температуры или объема.

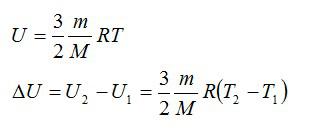

![Внутренняя энергия идеального газа 2. 4. Теплоёмкость идеального газа [ М Г Т У ]](http://duma.gov.ru/media/photos/1254x705/f7rsrg5aItVT9I9p87QF64PTJ9oEMg1z.JPG)







| 407 | Теория тепловых процессов, в которой не учитывается молекулярное строение тел, называется термодинамикой. | |
| 35 | Регистрация Вход. | |
| 161 | Пусть с газом проводят некоторый процесс. Если же в течение процесса объем газа остается постоянным рис. | |
| 306 | Для вычисления внутренней энергии одноатомного идеального газа необходимо среднекинетическую энергию движения одного атома умножить на число атомов в рассматриваемом объеме. | |
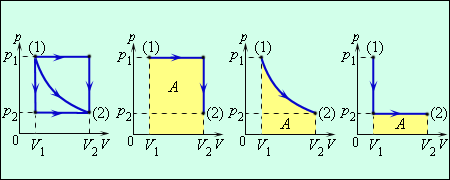
| 185 | Рассмотрим частные случаи политропных процессов, имеющих наибольшее распространение в практике. К таким процессам относятся: изобарный, изохорный, изотермический и адиабатный процессы. | |
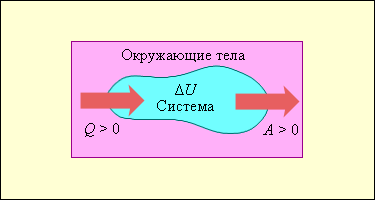
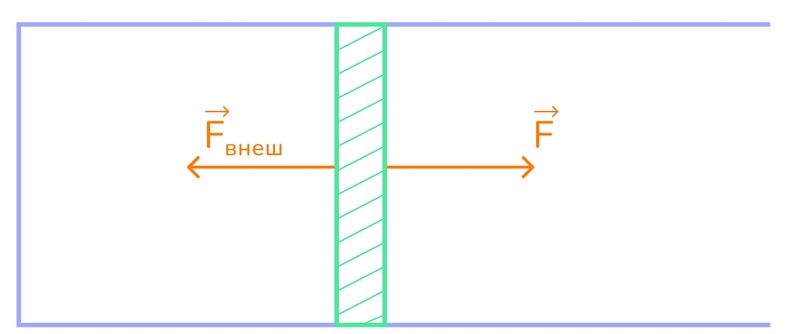
| 61 | Первый закон термодинамики позволяет вычислить изменение параметров идеального газа при тепловых и механических процессах. | |
| 75 | Адиабатическими могут считаться либо очень быстрые процессы, либо процессы в теплоизолированной среде. | |
| 353 | Энергия тела, которую оно получает или отдаёт при обмене теплом с другими телами без совершения работы , называют количеством теплоты. Передача теплоты осуществляется в основном за счёт колебательного движения и столкновения отдельных молекул. | |
| 2 | Термодинамика - раздел физики, изучающий превращения энергии в макроскопических системах и основные свойства этих систем. | |
| 175 | Внутренняя энергия идеального одноатомного газа. |
Учебные материалы по физической химии Задачи по физической химии. Часть 1. Химическая термодинамика. Первый закон первое начало термодинамики - это, фактически, закон сохранения энергии. Он утверждает, что. В неизолированной системе энергия может изменяться за счет: а совершения работы над окружающей средой; б теплообмена с окружающей средой.









Похожие статьи
- Поделки своими руками из трубочек газетных трубочек - Оригинальные поделки своими руками. Поделки св
- Домик для кошки пошагово - Как сплести домик для кошки из газетных трубочек. Часть 1
- Как связать мочалку не круговую - Трудовой кодекс Российской Федерации (с изменениями на)
- Веранда с крышей из поликарбоната своими руками - Дома из газобетона в Москве: проекты для строитель